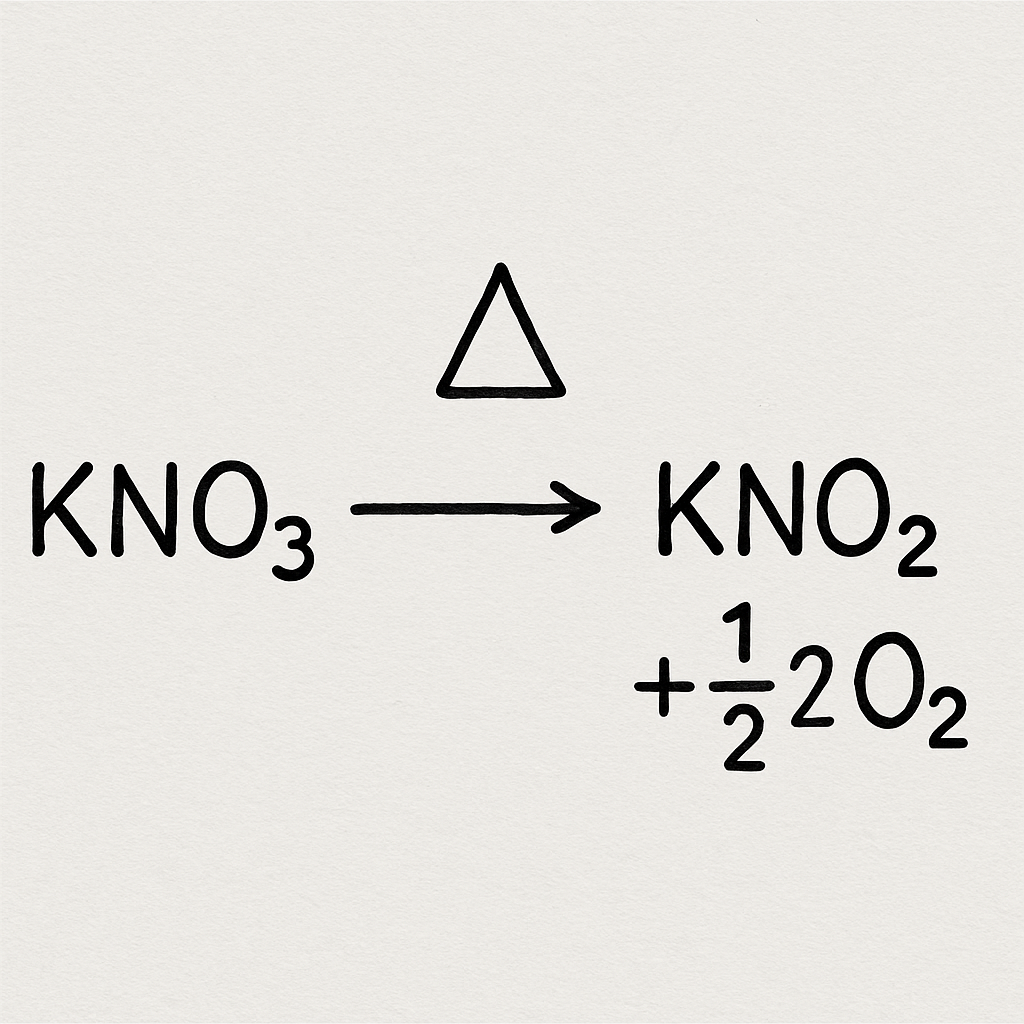نترات البوتاسيوم، المعروفة باسم ملح البارود، مركب كيميائي واسع الاستخدام في مختلف الصناعات. صيغته الكيميائية KNO3. يشتهر هذا المركب ليس فقط باستخدامه التاريخي في البارود، بل أيضاً بدوره في الأسمدة وحفظ الأغذية وحتى الألعاب النارية. يمكن أن تُنتج تفاعلات نترات البوتاسيوم مجموعة متنوعة من المنتجات المهمة، مما يجعلها مركباً قيماً في الكيمياء.
يتكون نترات البوتاسيوم من البوتاسيوم (K) والنيتروجين (N) والأكسجين (O). وهو ملح بلوري ويظهر على شكل مسحوق أبيض في صورته النقية. الذوبان في الماء وقدرته على العمل كعامل مؤكسد تجعله مفيدًا بشكل خاص في العديد من التفاعلات الكيميائية.
كيمياء نترات البوتاسيوم (KNO3)
على المستوى الجزيئي، يتكون نترات البوتاسيوم من أيون بوتاسيوم واحد (K+) وأيون نترات واحد (NO3-). أيون النترات متعدد الذرات، أي أنه يحتوي على عدة ذرات. ويلعب هذا الأيون دورًا رئيسيًا في التفاعلات المختلفة التي تشمل نترات البوتاسيوم.
تحلل نترات البوتاسيوم
من أكثر التفاعلات إثارةً للاهتمام التي تشمل نترات البوتاسيوم هو تحللها. فعند تسخين نترات البوتاسيوم، تتحلل إلى مركبات أبسط. هذا التحلل تفاعل ماص للحرارة، أي أنه يمتص الحرارة.
ماذا يحدث أثناء التحلل؟
يمكن تلخيص تحلل نترات البوتاسيوم بالمعادلة الكيميائية التالية:
2KNO3→2KNO2+O2
في هذا التفاعل، يتحلل نترات البوتاسيوم إلى نتريت البوتاسيوم (KNO2) وغاز الأكسجين (O2). يُعدّ انطلاق الأكسجين هذا ذا أهمية بالغة لأنه يُسهم في عملية الاحتراق، ولهذا السبب استُخدم نترات البوتاسيوم تاريخياً في صناعة البارود.
تفاعلات الأكسدة التي تتضمن KNO3
يُعرف نترات البوتاسيوم أيضاً بدوره في تفاعلات الأكسدة. وباعتباره عاملاً مؤكسداً، فإنه يستطيع استقبال الإلكترونات من مواد أخرى، مما يسهل حدوث تحولات كيميائية متنوعة.
نترات البوتاسيوم كعامل مؤكسد
في سياق تفاعلات الأكسدة، يمكن تمثيل نترات البوتاسيوم بشكل مبسط كما يلي:
2KNO3(s)+C(s)→2KNO2(s)+CO2(g)
في هذا التفاعل، يؤكسد نترات البوتاسيوم الكربون (C) إلى ثاني أكسيد الكربون (CO2)، بينما يُختزل هو نفسه إلى نتريت البوتاسيوم (KNO2). يُعد هذا النوع من التفاعلات أساسيًا في الألعاب النارية وغيرها من التطبيقات التي تتطلب أكسدة مُتحكم بها.
الاستخدامات العملية لنترات البوتاسيوم
إلى جانب خصائصه الكيميائية، يُعد نترات البوتاسيوم مركباً مهماً في العديد من التطبيقات العملية. وقد جعلته قدرته على المشاركة في التفاعلات الكيميائية ذا قيمة في مجالات عديدة.
الأسمدة والزراعة
في الزراعة، يُستخدم نترات البوتاسيوم كسماد نظراً لاحتوائه على نسبة عالية من النيتروجين والبوتاسيوم. هذه العناصر ضرورية لنمو النبات. يوفر مصدراً متاحاً بسهولة لهذه العناصر الغذائية, تعزيز نمو النباتات بشكل صحي.
حفظ الأغذية
يلعب نترات البوتاسيوم دورًا في حفظ الأغذية، حيث يُستخدم في معالجة اللحوم، ويساعد على منع نمو البكتيريا والحفاظ على لونها الوردي. ويخضع هذا الاستخدام لرقابة دقيقة لضمان سلامة الغذاء.
الألعاب النارية والمؤثرات البصرية
إن الطبيعة المتفجرة والمتفاعلة لنترات البوتاسيوم تجعلها عنصر أساسي في الألعاب النارية والمؤثرات البصرية. إن قدرتها على إطلاق الأكسجين أثناء التحلل تدعم الاحتراق السريع اللازم لخلق عروض نابضة بالحياة من الضوء واللون.
استكشاف المزيد من ردود الفعل
لا تقتصر كيمياء نترات البوتاسيوم على التحلل والأكسدة، بل يمكنها المشاركة في تفاعلات أخرى تُنتج نواتج مختلفة، وذلك تبعاً للظروف والمواد المتفاعلة.
التفاعل مع حمض الكبريتيك
عندما يتفاعل نترات البوتاسيوم مع حمض الكبريتيك المركز (H2SO4)، فإنه ينتج حمض النيتريك (HNO3) وبيكبريتات البوتاسيوم (KHSO4):
KNO3+H2لذا4→HNO3+KHSO4
يُستخدم هذا التفاعل صناعياً لإنتاج حمض النيتريك، وهو مادة كيميائية حيوية في عمليات التصنيع والمختبرات.
التفاعل مع الفحم
في الألعاب النارية والبارود، يُخلط نترات البوتاسيوم عادةً مع الفحم والكبريت. يخضع هذا المزيج لتفاعل طارد للحرارة سريع، ينتج عنه غازات تتمدد وتُحدث انفجارًا. المعادلة الكيميائية الموزونة لهذا التفاعل في البارود هي:
2KNO3+3C+S→K2S+3CO2+N2
يُظهر هذا تنوع استخدامات نترات البوتاسيوم في إحداث تفاعلات نشطة للتطبيقات العملية.
خاتمة
يُعدّ نترات البوتاسيوم مركباً ذا أهمية كيميائية وعملية بالغة. فقدرته على التحلل والأكسدة والمشاركة في تفاعلات متنوعة تجعله مورداً قيماً في العديد من الصناعات. من الزراعة إلى الألعاب النارية، ساهمت نواتج تفاعلات نترات البوتاسيوم في تشكيل استخداماته المتعددة. إن فهم هذه التفاعلات لا يُبرز فقط تنوع استخدامات نترات البوتاسيوم، بل يُؤكد أيضاً دوره في تطوير العمليات العلمية والصناعية. سواء في المختبر أو في الحقل أو في السماء، يبقى نترات البوتاسيوم مركباً جديراً بالاستكشاف.